HistoSonics, fabricant du système d’histotripsie Edison®, a annoncé aujourd’hui que Highmark Blue Cross Blue Shield a pris quatre décisions médicales positives concernant l’utilisation de l’histotripsie dans le traitement des tumeurs hépatiques. Cette décision élargit la prise en charge des contrats commerciaux de Highmark à quatre États — New York, Delaware, Pennsylvanie et Virginie-Occidentale —, offrant ainsi l’accès à la thérapie non invasive d’HistoSonics à environ 7 millions de personnes.
Ce communiqué de presse contient des éléments multimédias. Voir le communiqué complet ici : https://www.businesswire.com/news/home/20250714093378/fr/
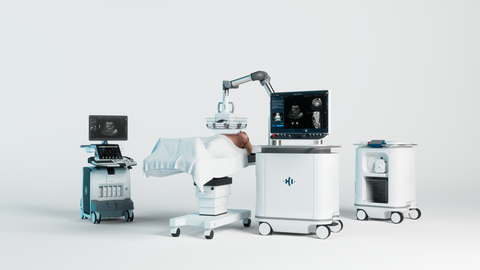
HistoSonics Non-Invasive Edison Histotripsy System
Le système Edison Histotripsy, autorisé par la FDA sous procédure De Novo en octobre 2023, utilise des ultrasons focalisés non invasifs pour détruire mécaniquement les tissus ciblés, les liquéfier au niveau subcellulaire, et ce, sans les risques ni la toxicité des traitements traditionnels. À ce jour, près de 2 000 patients ont bénéficié de l’histotripsie dans plus de cinquante établissements médicaux majeurs aux États-Unis, aux Émirats arabes unis et à Hong Kong. Les données cliniques, notamment celles de l’étude #HOPE4LIVER, ont démontré un taux de contrôle local des tumeurs de 90 % à 12 mois pour tous les types de tumeurs traités — un résultat nettement supérieur aux thérapies existantes, renforçant l’intérêt des assureurs.
« Cette extension de prise en charge par Highmark représente une avancée majeure pour permettre à davantage de patients d’accéder à une option sûre et non invasive », a déclaré Mike Blue, président-directeur général de HistoSonics. « Cette décision témoigne non seulement de la valeur clinique de notre technologie, mais elle renforce aussi la confiance des assureurs alors que nous poursuivons notre mission d’élargir son accès à l’échelle nationale. »
La décision de Highmark, effective depuis le 1er juillet 2024, s’ajoute à la liste croissante d’assureurs commerciaux qui reconnaissent la sécurité et l’efficacité de l’histotripsie, suivant ainsi l’exemple de Blue Cross Blue Shield of Michigan. Par ailleurs, l’United Network for Organ Sharing (UNOS) reconnaît désormais l’histotripsie comme une thérapie loco-régionale approuvée pour les patients en attente de greffe hépatique.
Le système Edison® est conçu pour la destruction mécanique non invasive des tumeurs hépatiques, y compris l’ablation partielle ou complète de tumeurs inopérables grâce à l’histotripsie. La FDA n’a pas encore évalué le système Edison pour le traitement d’une maladie spécifique, y compris le cancer, ni validé des résultats cliniques comme le contrôle tumoral local, la survie à cinq ans ou la survie globale.
Le dispositif ne doit être utilisé que par des médecins ayant suivi la formation HistoSonics, son utilisation devant reposer sur le jugement clinique d’un professionnel qualifié. Pour consulter l’ensemble des mises en garde, précautions, résultats d’essais cliniques et événements indésirables, veuillez vous référer au mode d’emploi du dispositif.
À propos de HistoSonics
HistoSonics est une société privée spécialisée dans les dispositifs médicaux, qui développe une plateforme thérapeutique non invasive reposant sur l’histotripsie : un mécanisme d’action innovant utilisant des ultrasons focalisés pour détruire mécaniquement et liquéfier les tissus indésirables et les tumeurs. L’entreprise concentre actuellement la commercialisation du système Edison aux États-Unis et sur certains marchés internationaux pour le traitement des affections hépatiques, tout en poursuivant le développement d’applications sur d’autres organes tels que les reins, le pancréas et la prostate. HistoSonics est implantée à Ann Arbor (Michigan) et à Minneapolis (Minnesota). Pour plus d’informations sur le système Edison Histotripsy : www.histosonics.com. Pour les patients : www.myhistotripsy.com.
Le texte du communiqué issu d’une traduction ne doit d’aucune manière être considéré comme officiel. La seule version du communiqué qui fasse foi est celle du communiqué dans sa langue d’origine. La traduction devra toujours être confrontée au texte source, qui fera jurisprudence.
Consultez la version source sur businesswire.com : https://www.businesswire.com/news/home/20250714093378/fr/
© Business Wire, Inc.
Avertissement :
Ce communiqué de presse n’est pas un document produit par l’AFP. L’AFP décline toute responsabilité quant à son contenu. Pour toute question le concernant, veuillez contacter les personnes/entités indiquées dans le corps du communiqué de presse.
